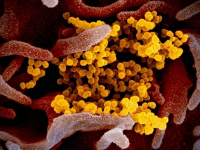
芝加哥大学化学家的研究发现了艾滋病毒自我复制过程中的一个新的关键步骤。
这项研究发表在1月6日的《科学进展》(Science Advances)杂志上,利用计算机建模重点研究了艾滋病毒是如何形成携带其遗传物质的胶囊的——特别是一种被称为IP6的特殊离子的作用。科学家们此前曾怀疑IP6具有重要功能,但不知道它究竟是如何工作的。
这个理论可以解释一种有前途的新药成功的某些方面,也可以为其他治疗方法指明方向。
多年来,我们已经知道艾滋病毒是艾滋病背后的危险病毒,但我们对它进入人体后的确切行为知之甚少。解开一系列复杂的生化事件可以告诉我们在哪里以及如何对抗病毒。
艾滋病毒携带它的遗传物质在一个被称为衣壳的小胶囊里。
“这种衣壳多年来一直是艾滋病毒研究人员的目标,”芝加哥大学海格·p·帕帕齐安化学杰出服务教授、该论文的资深作者格雷戈里·沃斯说。“我们的想法是,如果我们能阻止衣壳的形成,或者使它们畸形,我们就可以防止艾滋病毒的传染性和复制。”
衣壳由大约一千种蛋白质组成,形成六面或五面形状,它们像砖块一样组装成一个封闭的结构。科学家们知道一种名为IP6的离子在这一过程中也很重要,但不清楚原因。
对于沃斯教授的研究小组来说,这是一个完美的问题,他们擅长使用计算机模拟来理解复杂分子的行为。
这篇论文的第一作者,博士生Manish Gupta建立了一个HIV衣壳成分的模型。然后,研究小组进行了多次模拟,略有不同的变化,以找出衣壳是如何组装的,以及哪些部分是关键的。
从他们之前的研究中,研究小组知道IP6离子倾向于位于五面结构的中间。但他们的新模拟显示,在衣壳组装过程中,一些IP6离子必须结合到这些五面结构中,以便在很早的时候稳定它们,以便最终闭合。
Voth解释说:“当衣壳开始组装时,这些五面结构创造了一个高曲率区域,衣壳需要最终关闭末端。”“如果它们不这样做,这个结构就会开始形成一个两端都是开放的管子,而且它无法关闭。”
https://news.uchicago.edu/sites/default/files/video/movie_S2_ca-ip6_AdobeExpress.mp4
模拟显示了HIV蛋白质如何聚集在一起形成一个胶囊来存储其遗传物质。科学家们发现,一种叫做IP6的特殊离子(黄色部分)在闭合胶囊末端的过程中起着关键作用,这可能为治疗提供了一种途径。模拟由Gupta, Pak & Voth提供。
如果这个过程的结果是管状而不是封闭的形状,遗传物质就不能被封闭,不能被带到下一个目标。病毒复制失败。
尽管IP6很小,只影响数百个相关分子中的12个,但它在这个过程中发挥着巨大的作用。
“IP6也需要从一开始就参与进来。这有点像飙车;如果你在起跑线上的速度不合适,你就完了。”沃斯说。
重要的发现
这一结果可能解释了目前正在进行人体试验的药物lenacapavir的前景。Lenacapavir与IP6“竞争”,使六面结构比五面结构更稳定。这使得这个过程倾向于开放的管状结构,而不是封闭的衣壳。
“这是一个非常令人兴奋的结果。任何对病毒组装至关重要的东西都可能成为药物靶点,所以我们一直在寻找这些关键阶段。”沃斯解释说。
沃斯还说,研究小组有兴趣发现这一过程是否更普遍地适用于艾滋病毒以外的病毒。“也许这些‘次要’参与者比我们想象的更重要。”他说。
这些是极其复杂的模拟,涉及一百万个或更多的单个原子;它们必须在超级计算机上执行。这些测试是在德克萨斯大学奥斯汀分校的德克萨斯高级计算中心(TACC)的Frontera超级计算机上进行的。
这项研究的另一位作者是亚历山大·帕克(Alexander Pak),他曾是芝加哥大学的博士后研究员,现在就职于科罗拉多矿业学院。
引用本文:“HIV-1病毒衣壳组装的关键机制特征。”Gupta, Pak和Voth,科学进展,2023年1月6日。
资助:美国国立过敏和传染病研究所,国立卫生研究院。
注:本文由院校官方新闻直译,仅供参考,不代表指南者留学态度观点。