指南者留学全国统一咨询热线:400-183-1832,全国各地区、各分公司联系方式均为此号码。
这项发表在《癌症发现》杂志上的研究,描述了一种新的方法,使用在特别设计的3D“支架”中生长的人类干细胞,生成存在于人类骨髓中的关键细胞类型(骨髓是持续生产循环血细胞的工厂)。
这些新的类器官还可以让血癌患者的癌细胞在实验室中存活,这在以前是非常困难的。这意味着医生现在可以在特定患者的癌细胞上测试定制的治疗方法,以找到最有可能治疗癌症的治疗方法。
伯明翰大学心血管科学研究所亨利·威康爵士研究员阿卜杜拉·汗博士是该研究的第一作者,他说:“值得注意的是,我们发现他们骨髓类器官中的细胞与真正的骨髓细胞相似,不仅在活性和功能方面,而且在结构关系方面——细胞类型在类器官中‘自我组织’和排列自己,就像他们在人体内的骨髓中那样。”
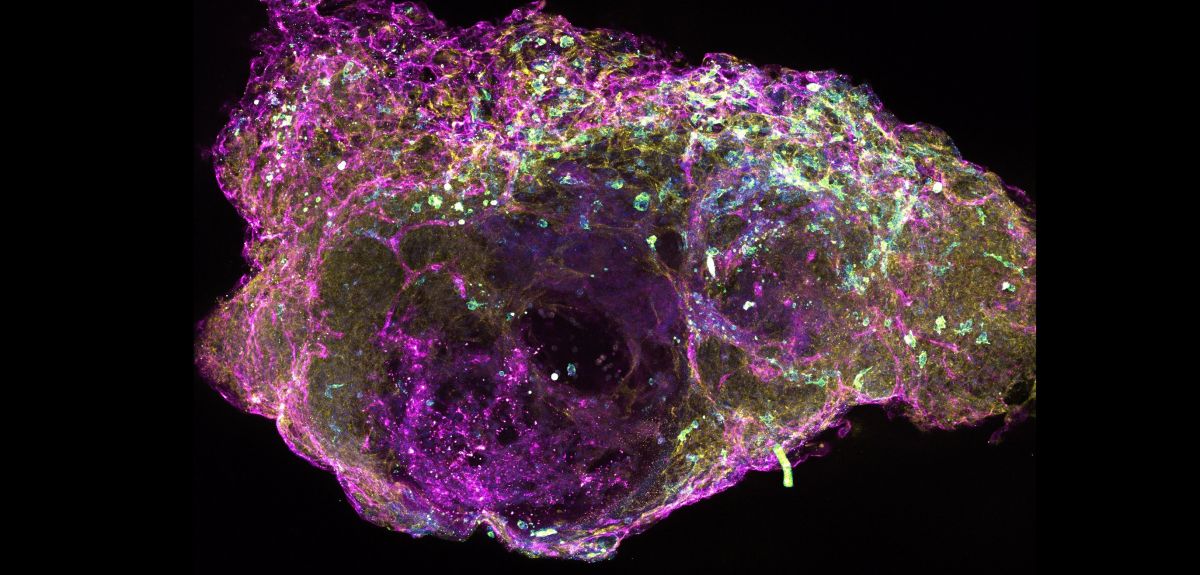
这种栩栩如生的结构使研究小组能够研究骨髓中的细胞如何相互作用以支持正常血细胞的产生,以及在骨髓纤维化(也称为骨髓纤维化)中这是如何受到干扰的,在骨髓纤维化中疤痕组织积累,导致骨髓衰竭。骨髓纤维化可在某些类型的血癌患者中发生,而且仍然无法治愈。
血癌是影响儿童的最常见癌症,也是影响成人的十大最常见癌症之一。在成人中,它们基本上无法治愈。
该研究的资深作者、牛津大学拉德克利夫医学院血液学医学博士、研究小组负责人贝than Psaila教授说:“为了正确理解血癌是如何以及为什么发展的,我们需要使用与真正的人类骨髓工作原理非常相似的实验系统,这是我们以前从未有过的。”现在有了这个了不起的系统真是令人兴奋,因为我们终于能够直接使用患者的细胞来研究癌症,而不是依赖动物模型或其他更简单的系统,这些系统不能正确地向我们展示癌症在实际患者骨髓中是如何发展的。”
Khan博士还补充说:“这是向前迈出的一大步,使我们能够深入了解癌细胞的生长模式,并有可能实现更个性化的治疗方法。”
“制定一种方案,让我们能够大规模地重复种植类器官是一项挑战,特别是我们在伯明翰和牛津的实验室之间合作应对疫情,所以我花了很多时间疯狂地在A40公路上驾驶类器官。”然而,我们对结果感到兴奋,因为我们现在有了一个平台,可以在“个性化药物”的基础上测试药物。
“开发和验证该模型是关键的第一步,在我们正在进行的合作工作中,我们将与其他人合作,更好地了解健康人群的骨髓是如何工作的,以及当他们患有血液疾病时,是什么出了问题。”
Psaila博士补充说:“我们希望这项新技术将有助于加速新的血癌治疗方法的发现和测试,使改进后的药物更快地进入临床试验。”
这篇论文的全文,“用于疾病建模的人类骨髓类器官,发现和验证血液系统恶性肿瘤的治疗靶点”,可以在《癌症发现》上阅读。
注:本文由院校官方新闻直译,仅供参考,不代表指南者留学态度观点。